
人教版九年级化学上册《原子的结构》PPT精品课件(第2课时),共40页。《原子的结构》PPT精品课件包含课前回顾、新课讲授、小结、典型例题等内容。质子数 决定元素的种类最外层电子数决定元素的化学性质(1)稀有气体元素:最外层电子数为8个(He 为2个),化学性质稳定,这种结构称为稳定结构;(2)金属元素:最外层电子数少于4个,易失去电子,化学性质活泼;(3)非金属元素:最外层电子数大于或等于4个,易得到电子,化学性质活泼。结论:结构决定性质。离子也是构成物质的粒子。阴、阳离子由于静电作用而形成不

人教版九年级化学上册《原子的结构》PPT精品课件(第1课时),共35页。《原子的结构》PPT精品课件包含课前回顾、阅读课本思考、典型例题、课堂反馈、本节收获等内容。授课内容1、构成原子的微粒有三种:质子、中子、电子.决定原子种类的是:质子数(所有原子都是三种粒子构成原子吗?有没有例外?)2、原子中:核电荷数=质子数=核外电子数3、原子不显电性的原因:原子是由居于原子中心带正电的原子核和核外带负电的电子构成,原子核又是由质子和中子构成,质子带正电,中子不带电;原子核所带的正电荷数(核电荷数)和核外

《原子的结构》物质构成的奥秘PPT(第2课时),共16页。导入新课科普小论文《漫游原子世界》我是一个小小的电子,我在原子内围绕着原子核不停地转动,虽然空间很大,但我和我的同伴总想挣脱原子核的吸引。可是原子核这个“小老头”很有能耐,虽然只占原子的一丁点空间(相当于体育场中的小蚂蚁),它却由质子和中子构成,中子不带电,质子带正电,正好将我身上的负电深深吸引。大家猜一猜,我和我的同伴在原子里是怎样运动的呢?学习目标1.知道原子核外电子是分层排布的2.了解原子结构示意图的含义;了

《原子的结构》物质构成的奥秘PPT(第1课时)。共19元。导入新课观察与思考通过图片,你获得了哪些信息?学习目标1.了解原子是由质子、中子、电子构成的2.初步了解相对原子质量的概念,并学会查相对原子质量表 讲授新课原子的构成观察与思考观察图片,你发现了什么?1.原子不是一个实心球体;2.原子是由居于原子中心的原子核和核外电子构成的;3.原子核带正电荷,电子带负电荷。交流与讨论(1)一个质子和一个电子所带的电量相等,电性相反。(2)一个质子和一个中子的质量约相等。(3)原子的质

《原子的结构》物质构成的奥秘PPT,共18页。学习三维目标能说出原子的结构;会解释原子不显电性的原因;知道原子的质量为什么主要集中在原子核上。 原子构成的发现史1.电子的发现十九世纪末前,原子一直被认为是坚硬不可分割的实心球体。 1897年,在英国科学家汤姆森发现了电子,叩开了人们认识原子的大门。经过20世纪整整一个世纪的努力,科学家不但打开了原子的大门,而且发现小小的原子内部结构十分复杂。2.汤姆森对原子中带正电部分的猜想汤姆森的“葡萄干布丁”模型。

《原子的结构》物质构成的奥秘PPT课件4观察表格(表4-2),思考下列问题1、不同种原子之间有哪些区别?不同原子的质子数、中子、电子数都不同。2、所有原子都是由质子、中子、电子构成的吗?氢原子的中子数为0,因此,不是所有的原子都有中子。3、质子、中子、电子在数量上有什么关系?质子数一定等于电子数,但不一定等于中子数。4、原子本身带电吗?为什么?质子和电子数目相等、电性相反,互相抵消 ,所以原子不带电。 一、原子的构成原子核质子(带正电)中子(不带电)核外电子(带负电)核电荷数

《原子的结构》物质构成的奥秘PPT课件6复习提问1.分子和原子的定义?2.分子和原子的特征?3.化学反应的实质?在化学反应里分子可以分为原子,原子不能再分,那么用其它方法能不能将原子再分呢?1897年,英国科学家汤姆生发现了电子(来自原子内部),证明原子可分的;卢瑟福提出原子结构的“核式模型”又叫“行星模型” 一、原子的构成原子核质子中子核外电子1 电性和电量1个质子带一个单位正电荷;1个电子带一个单位负电荷。原子核所带的正电荷

《原子的结构》物质构成的奥秘PPT课件2一、学习目的:1.能说出构成原子的各种粒子及带电情况。(重点)2.知道相对原子质量表示的意义,会查相对原子质量表。(难点)卢瑟福得出结论:①原子核很小,原子内部有很大的空间②原子中心有个带正电荷的原子核,α粒子途径金原子核附近受到斥力改变了运动方向;③原子核质量比α粒子大,α粒子碰撞到原子核是被弹了回来 二、自主学习:知识点一:原子的结构发现史卢瑟福实验得出结论:①原子核很_____,原子内部有很__

《原子的结构》物质构成的奥秘PPT课件【情景激活】原子还可以再分吗?原子究竟是什么样子呢?今天,咱们就来畅游原子的世界!科学史话——原子结构的探索历程1803年,道尔顿提出:构成物质的最小粒子是原子,原子是不可再分的实心球体。1897年,汤姆生在原子内部发现了电子,人们终于抛弃了原子不可分割的陈旧观念。1911年,卢瑟福通过精密的实验证明在原子中心有一个极小的核,电子绕核做高速旋转。 原子是怎样构成的? 【智慧阅读】结合原子结构的探索历程,阅读书P53

《原子的结构》物质构成的奥秘PPT课件5学习目标1、了解原子的结构,知道原子的微观构成。2、了解原子核外电子的排布,知道离子的形成过程。3、知道相对原子质量的概念和计算公式。近代科学原子论(1803年)一切物质都是由最小的不能再分的粒子——原子构成。原子模型:原子是坚实的、不可再分的实心球。原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)电子是种带负电、有一定质量的微粒,普遍存在于各种原子之中。汤姆生原子模型:原子是一个平均分布着正
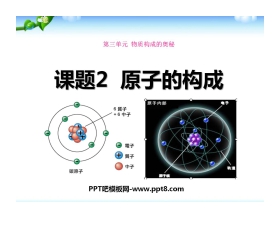
《原子的结构》物质构成的奥秘PPT课件3知识回顾在过氧化氢分解制氧气的实验中,过氧化氢____破裂为氢____和氧____ ,该反应的文字表达为:________________。可见,分子很小,但在化学反应中可以____ ,而____在化学变化中不可再分,所以说____________________是化学变化中的最小的粒子。(提示:填“分子”或“原子”)一、原子的构成1、原子的结构原子核质 子(带正电)中 子(不带电)电 子(带负电)观察表格(